- CABD
- Departamentos
- Biología celular y Biotecnología
- Regulación génica y morfogénesis
- Servicios científico-técnicos
- Servicios generales
- Noticias y divulgación
Biología celular y Biotecnología

Desarrollo del sistema hemato-vascular y células madre
Dra María José Sánchez Sanz
Investigador/a Principal Resumen
Publicaciones relevantes
Miembros del laboratorio y Colaboradores
Lista completa de publicaciones
Resumen
El empleo de células madre y células progenitoras en aplicaciones terapéuticas está limitado por la falta de información precisa sobre su comportamiento en procesos como mantenimiento de la homeostasis y en trasplantes. Los progenitores y células madre fetales presentan características distintivas comparados con células equivalentes del adulto, incluyendo su potente capacidad de repoblación en trasplantes. La investigación en células con características fetales es, por tanto, un tema de alto interés en el campo de estudio sobre las células madre. Nuestro trabajo está centrado en el análisis de los progenitores hematopoyéticos y vasculares derivados del hígado fetal y usamos el ratón como modelo experimental.
Líneas de investigación
1- Progenitores hemato/vasculares fetales versus adultos.
2- Notch y HSCs durante el desarrollo.
3- Desarrollo de modelos de terapia celular empleando progenitores hemato/vasculares fetales: La hemofilia A.
2- Notch y HSCs durante el desarrollo.
3- Desarrollo de modelos de terapia celular empleando progenitores hemato/vasculares fetales: La hemofilia A.
1- Progenitores hemato/vasculares fetales versus adultos. Hemos identificado un nuevo progenitor hemato/vascular fetal caracterizado por su alta capacidad de injerto comparado con células equivalentes obtenidas de adulto. También hemos determinado el momento y localización de su aparición durante el desarrollo embrionario así como, establecido un sistema de cultivo de órgano para su expansión ex vivo. Estos estudios proporcionan un marco de trabajo para abordar la investigación sobre las señales y mecanismos moleculares involucrados en procesos de generación, proliferación e injerto.
2- Notch y HSCs durante el desarrollo. Estudiamos la diferente capacidad de injerto de HSCs fetales y adultas en respuesta a la activación de la ruta de señalización de Notch empleando células aisladas de transgénicos SCL-NIC. Los resultados de estos estudios podrían ser de interés en el diseño de tratamientos dirigidos a los diferentes tipos de HSC en enfermedades de la sangre.
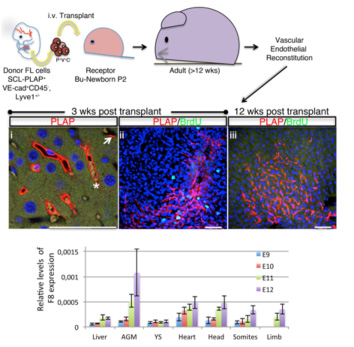
3-Desarrollo de modelos de terapia celular empleando progenitores hemato/vasculares fetales: La hemofilia A. Buscamos aplicaciones de los progenitores hemato/vasculares fetales en el desarrollo de modelos de terapia celular, en particular para el tratamiento en estadios de recién nacidos. Una de las líneas de investigación está enfocada en la hemofilia A, una enfermedad causada por la deficiente producción de factor de coagulación FVIII en células endoteliales vasculares y hematopoyéticas. Hemos determinado que el FVIII se expresa en estadios tempranos del desarrollo y en progenitores hemato/vasculares del hígado fetal. Actualmente estamos investigando si el trasplante de estos progenitores en mutantes F8 rescata el fenotipo.
Empleando diferentes técnicas como el uso de líneas transgénicas para marcaje de progenitores y seguimiento en trasplantes, FACS, análisis de imagen, cultivos y diversos modelos de trasplantes, intentamos descifrar las propiedades de los progenitor fetales a nivel celular y molecular con el objetivo a largo plazo, de entender su función en mantenimiento de la homeostasis y mejorar su uso en aplicaciones terapéuticas.
También en esta web:
CABD - Centro Andaluz de Biología del Desarrollo
Universidad Pablo de Olavide
Carretera de Utrera km1
41013 Sevilla, España
+34 954977911









© CABD 2008-2024 - CMS by BLWorks.net